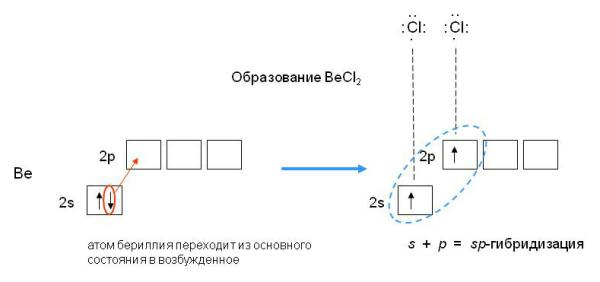
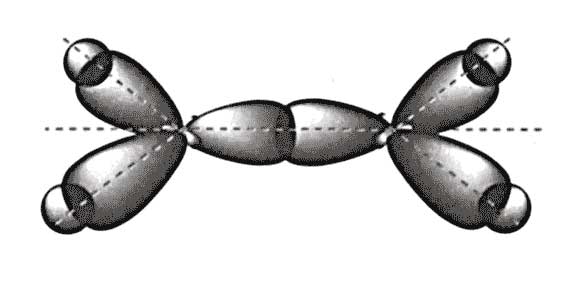
2.1. Ковалентная связь. Метод валентных связей
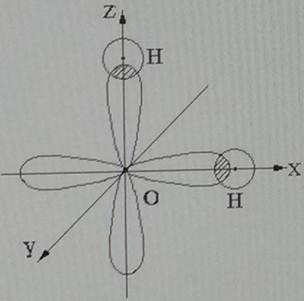
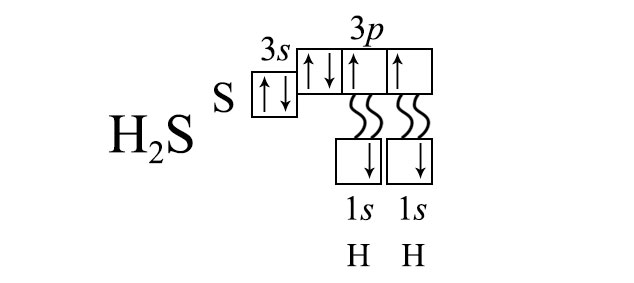
Молекула воды состоит из атома кислорода и двух атомов водорода. Два неспаренных р-электрона атома кислорода занимают две орбитали, которые располагаются под углом 90 o друг к другу. При образовании молекулы воды орбиталь каждого р-электрона перекрывается орбиталью s — электрона атома водорода рис. Схема перекрывания электронных орбиталей при образовании химических связей в молекуле воды. Угол между связями должен быть близок к углу между облаками р-электронов, то есть к 90 о.


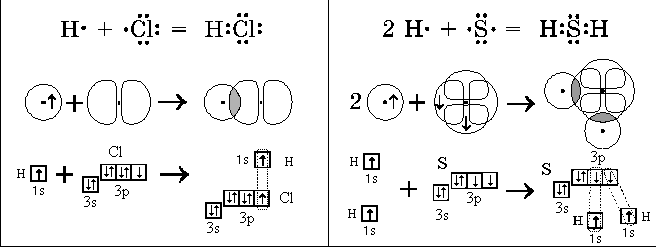


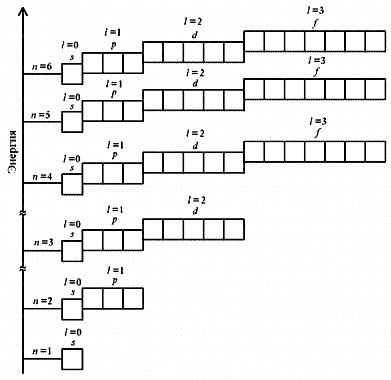

Глинка, Н. Задачи и упражнения по общей химии. Коровин, Н.



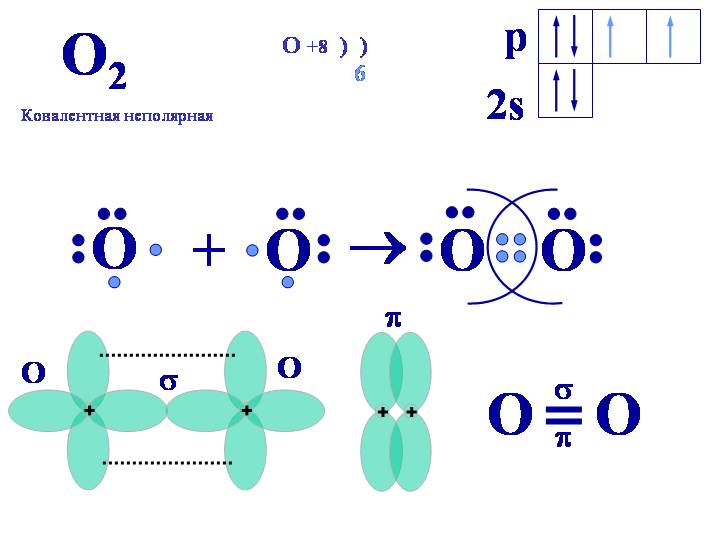



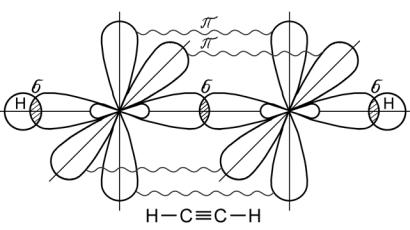
В годах Ф. Хунд, Дж. Леннард- Джонс и Р. Малликен развили идею нового подхода к поиску волновой функции молекулы, известного под названием метода молекулярных орбиталей МО. Он является наиболее универсальным квантовомеханическим методом описания химической связи.