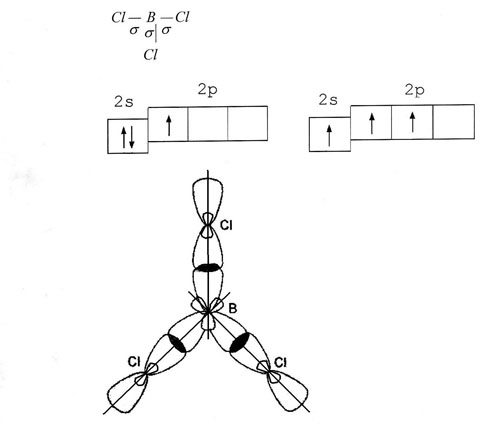
§ 14.1. Гибридизация атомных орбиталей
Чтобы войти в систему и использовать все возможности "Академии Хана", пожалуйста, включите JavaScript в своём браузере. Внести пожертвование Войти Зарегистрироваться Поиск курсов, уроков и видеороликов. Hybridization and hybrid orbitals. О проекте Об этом видео Транскрипция. Такая гибриизация возникает, когда атом окружён тремя группами электронов. Создатели: Jay.






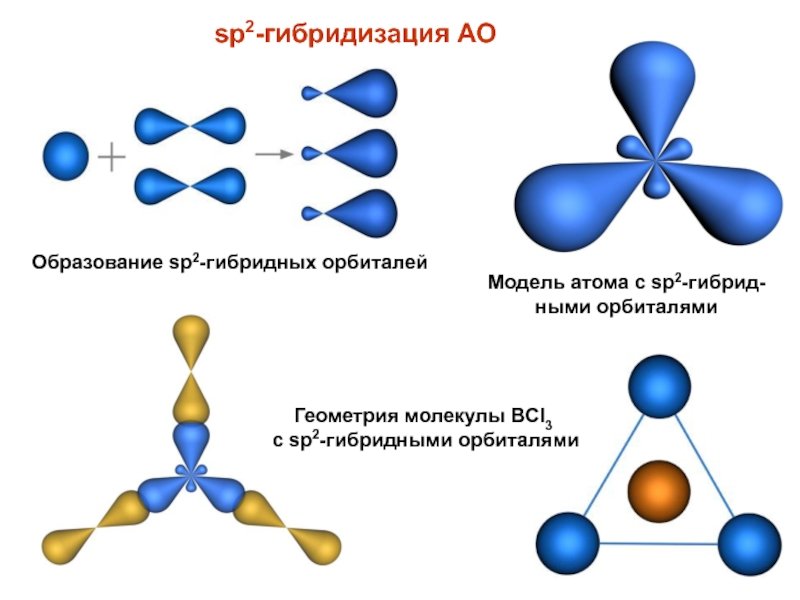
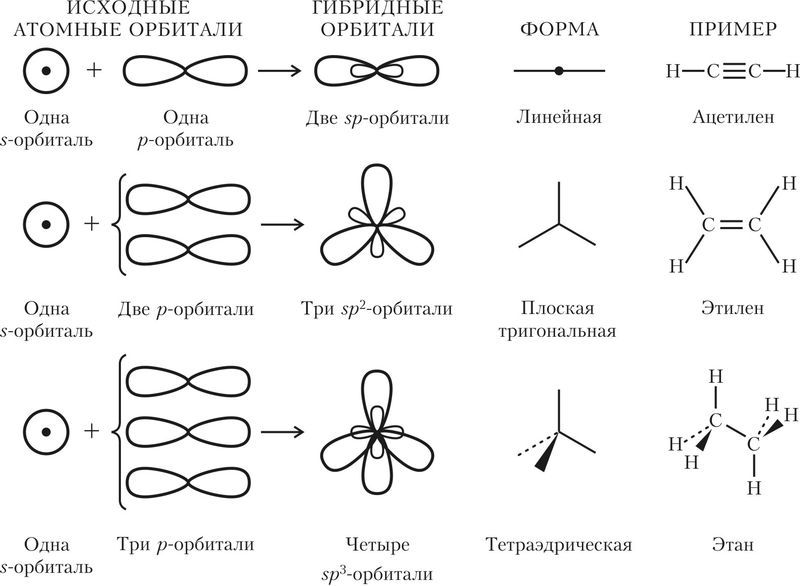

Удобная навигация, видео-разборы тем, задачи для самопроверки — всё это в вашем кармане. А ещё раздел с полезными материалами, календарь занятий и уведомления о предстоящих уроках. Понятие г ибридизации электронных орбиталей. Состояние валентных электронов описывает математическая модель гибридизации электронных орбиталей , которая предполагает не только выравнивание энергии, но и изменение формы орбитали, то есть смещение электронной плотности относительно ядра. Типы гибридизации атомов углерода.
- Стадия вызова 7 минут Организационные дейстия
- Краткосрочный поурочный план «Типы гибридизации: sp -, sp 2-, sp
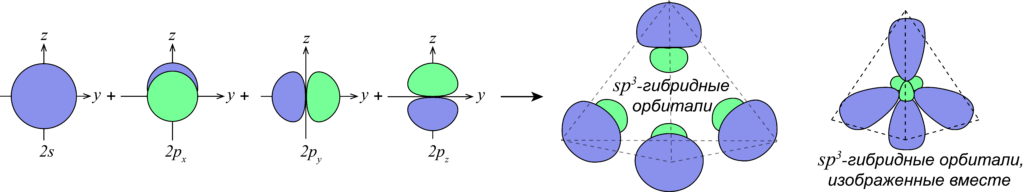
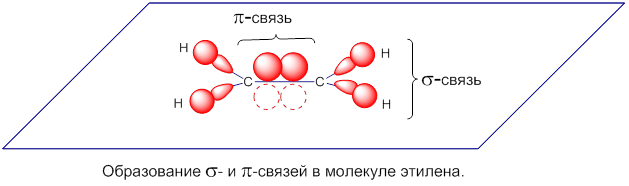
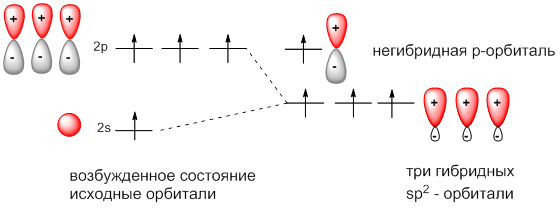
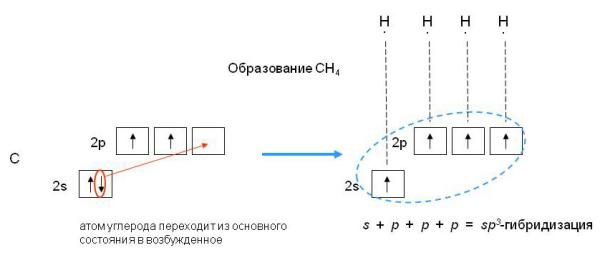
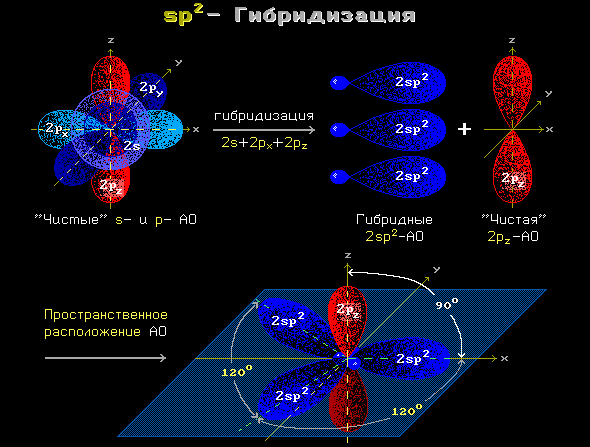
- Гибридизация — выравнивание смешивание атомных орбиталей s и р с образованием новых атомных орбиталей, называемых гибридными орбиталями. Атомная орбиталь — это функция, которая описывает плотность электронного облака в каждой точке пространства вокруг ядра атома.
- На всякий случай предупреждаю: кто не знает, как написать электронное строение атома - добро пожаловать в первую и вторую часть этого урока.




/Eshchanov.files/image005.jpg)
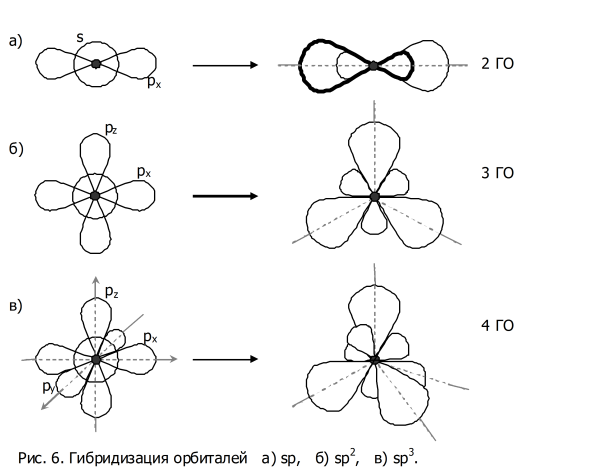
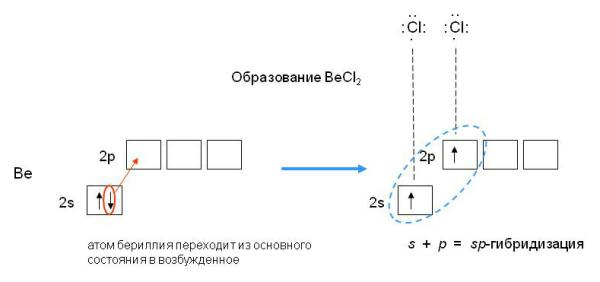

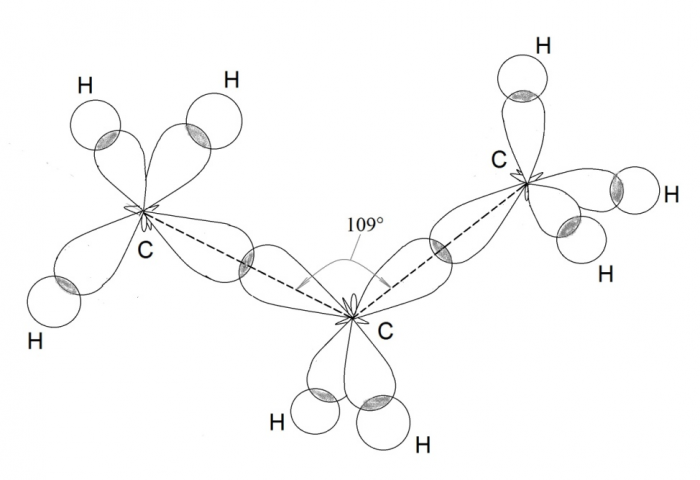
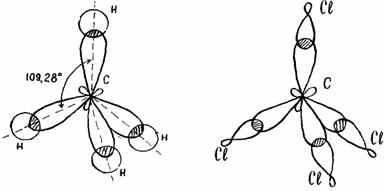
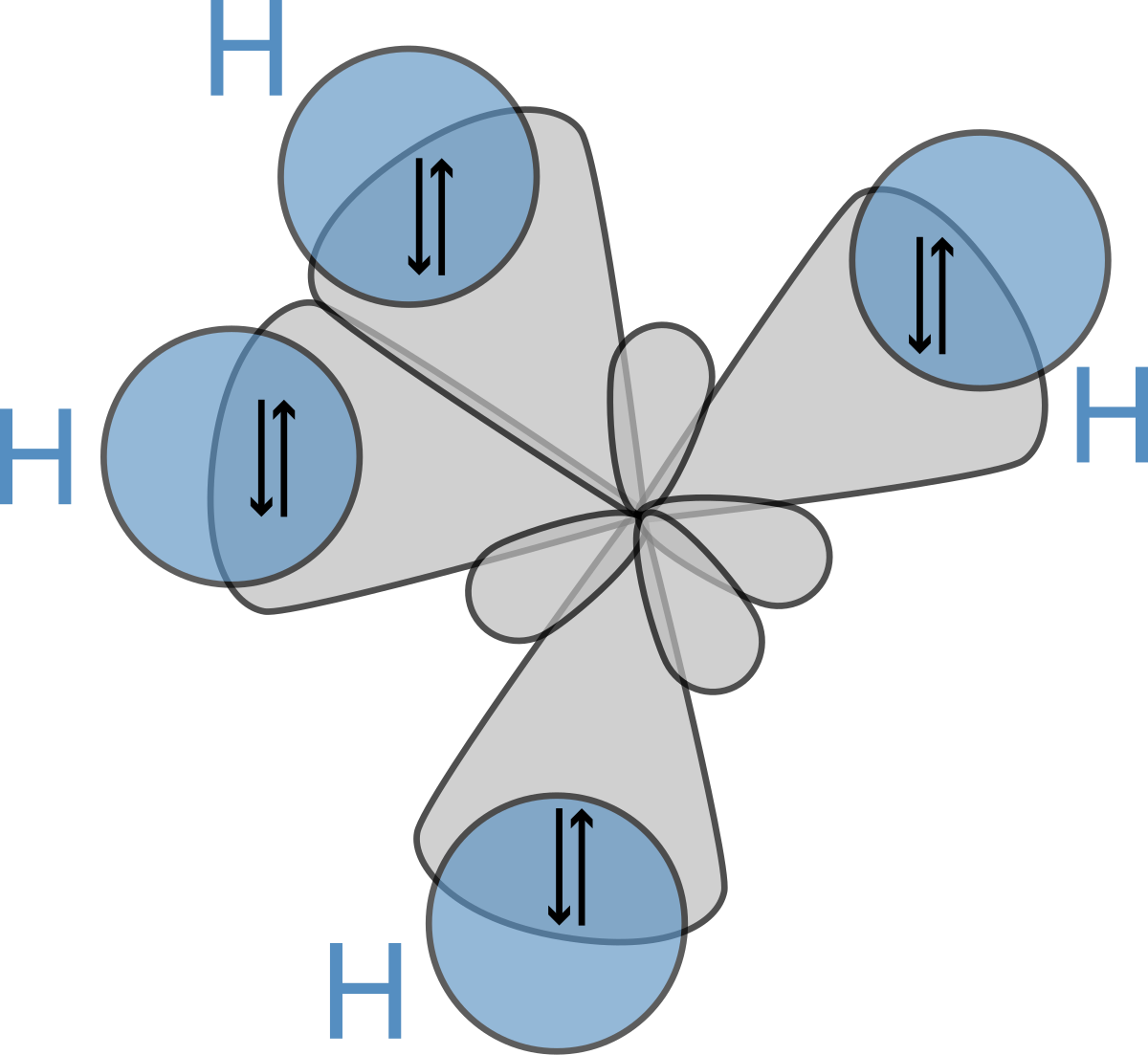
Угол между гибридными орбиталями при sp 3 -гибридизации равен Представления о гибридизации занимают центральное место в методе валентных связей. Сама гибридизация не является реальным физическим процессом, а только удобной моделью, позволяющей объяснить электронное строение молекул, в частности гипотетические видоизменения атомных орбиталей при образовании ковалентной химической связи , в частности, выравнивание длин химических связей и валентных углов в молекуле.